För drygt ett år sedan publicerades en retroaktiv studie på Attanas track record inom läkemedelsutveckling i IBI (International Biopharmaceutical Industry), läs hela artikeln här. Idag publiceras uppdaterade siffror där antalet läkemedelskandidater i den prekliniska fasen som Attana har analyserat ökat till 103 stycken jämfört med 77 stycken för drygt ett år sedan. De validerade kandidaterna har nu kommit längre i utvecklingsprocessen och framgången är fortsatt signifikant högre än branschsnittet.
Av de 103 analyserade kandidaterna har 36 validerats av Attana. 12 av de 36 validerade läkemedelskandidaterna har fått finansiering och påbörjat kliniska studier. Av dessa 12 har 7 tagit sig in i kliniska studier fas II, 2 har nyligen avslutat fas II och 3 befinner sig i den sista fasen, fas III. Av de 12 validerade kandidaterna som tagit sig in i kliniska studier har endast en avslutats, vilket var på grund av en inte tillräckligt ökad effekt jämfört med kontrollen.
Av de ”icke validerade” kandidaterna har en läkemedelskandidat fortsatt in i kliniska studier. I enlighet med Attanas prediktion uppvisade molekylen låg effekt i fas II och projektet har därför lagts ner.
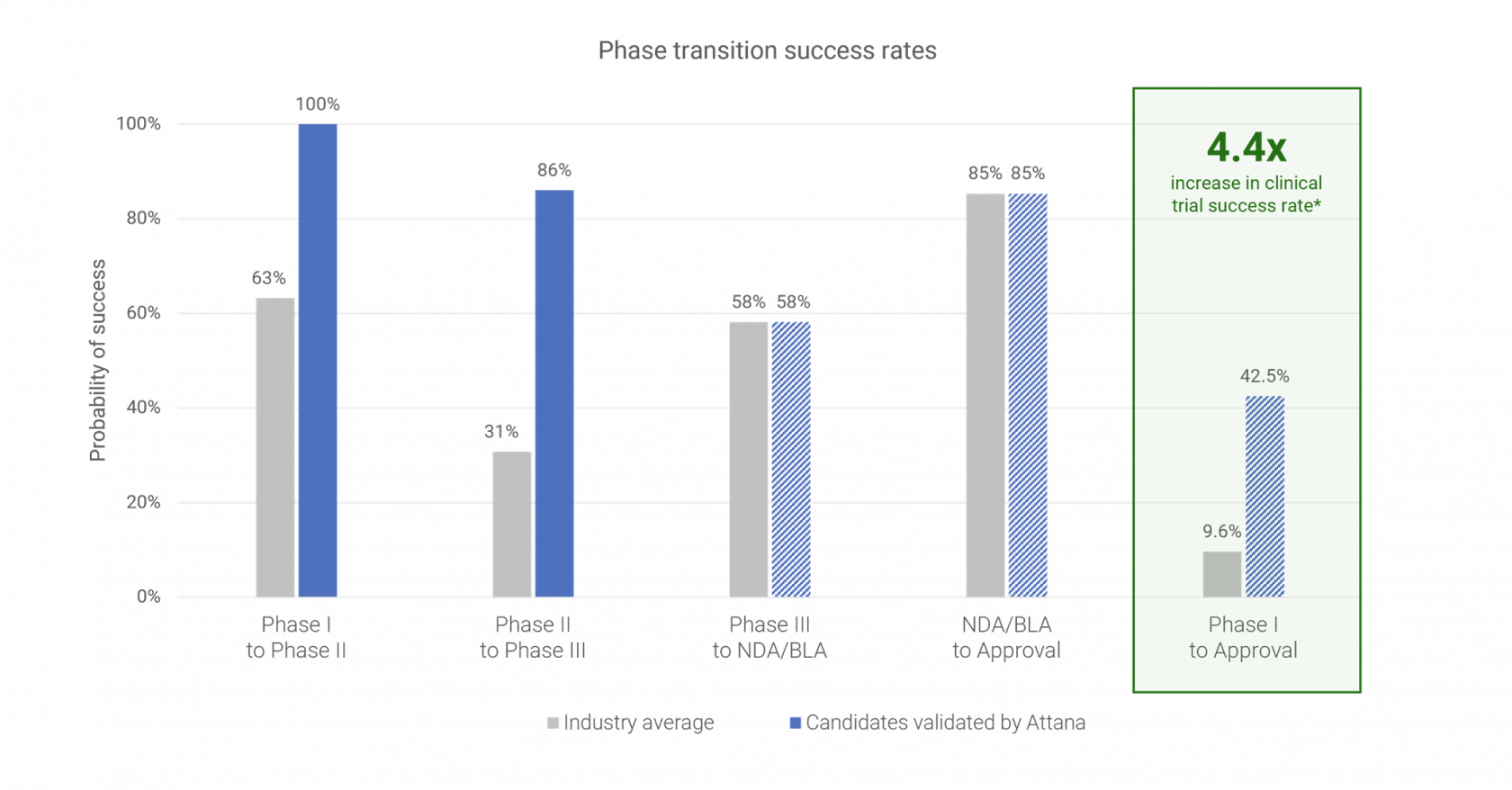
De uppdaterade resultaten visar på en 100% framgång för Attanas kandidater i övergången mellan fas I och II. Detta är avsevärt bättre än industrigenomsnittet på 63% vilket påvisar Attanas nytta som ett nytt tox-test. Även i övergången mellan fas II och fas III uppnår Attanas validerade kandidater en hög framgång på 86% jämfört med ett industrigenomsnitt på 31%. Samtliga kandidater i fas III påvisar hittills framgångsrika resultat. Sammantaget är Attanas validerade läkemedelskandidater 4,4 gånger mer framgångsrika i fas I & II som industrigenomsnittet.
Att utveckla läkemedel är extremt kostsamt. Den genomsnittliga FoU-kostnaden för ett läkemedel uppgår till ca. 2 miljarder dollar, varav ungefär hälften är relaterade till de kliniska studierna. Trots att majoriteten av de kandidater som påbörjar kliniska studier når fas II är det endast 22% som når fas III och mindre än 10% som godkänns, främst på grund av bristfälliga tester och analyser i pre-kliniska faser.
VD, Teodor Aastrup kommenterar:
”Vi grundade Attana då vi var övertygade om att kunna förbättra framgången i kliniska studier genom att både studera target- och off-target interaktioner på ett relevant biologiskt sätt. Attanas validerade läkemedelskandidater påvisar tydligt vikten av att säkerställa effektiva interaktioner samt att eliminera off-target interaktioner.”
För ytterligare information, kontakta:
Teodor Aastrup, VD
teodor.aastrup@attana.com
+46 (0)8 674 57 00
Styrelsen för Attana AB bedömer att informationen i detta pressmeddelande ej är av kurspåverkande karaktär men att det alltjämt är av betydande vikt att enhetligt via offentliggörandet kommunicera informationen till bolagets intressenter.
Om Attana
Attana AB grundades 2002 med idén att effektivisera forskning och utveckling av nya läkemedel genom biologisk interaktionskarakterisering i realtid. Baserat på sina patenterade teknologier säljer bolaget uppdragsforskning och egenproducerade analysinstrument samt ett in vitro diagnostiskt (IVD) verktyg, Attana Virus Analytics (AVA), till läkemedelsbolag, bioteknikföretag och akademiska institutioner. Mer information om Attanas forskningstjänster och produkter finns på www.attana.com eller kontakta sales@attana.com